ARN (Ácido Ribonucleico)
El ARN es la sigla para ácido ribonucleico. Es un ácido nucleico que se encarga de trasladar la información genética del ADN con el fin de sintetizar las proteínas según las funciones y características indicadas.
El ARN está presente en el citoplasma de las células eucariotas y procariotas. Asimismo, el ARN está compuesto por una cadena simple que en ocasiones puede duplicarse.
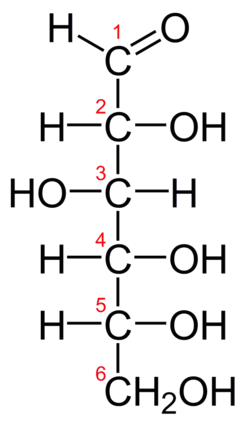
Está conformado por nucleótidos unidos que forman cadenas. Cada nucleótido está constituido por: un azúcar (ribosa), un grupo fosfato y 4 bases nitrogenadas (adenina, guanina, uracilo y citosina).
El ARN transporta la información genética del ADN para la síntesis de las proteínas necesarias. Es decir, el ARN copia la información de cada gen del ADN y, luego pasa al citoplasma, donde se une al ribosoma para dirigir la síntesis proteica.
El ARN comienza a ser estudiado en el año 1868 por Friedrich Miescher, asimismo, fue la primera persona en investigar el ADN y promover el estudio de los ácidos nucleicos.
La abreviación internacional es RNA por sus siglas en inglés para ribonucleic acid.
Tipos de ARN
En referencia a lo anterior, se puede distinguir la interacción de diversos tipos de ARN en la expresión genética, entre los cuales tenemos:
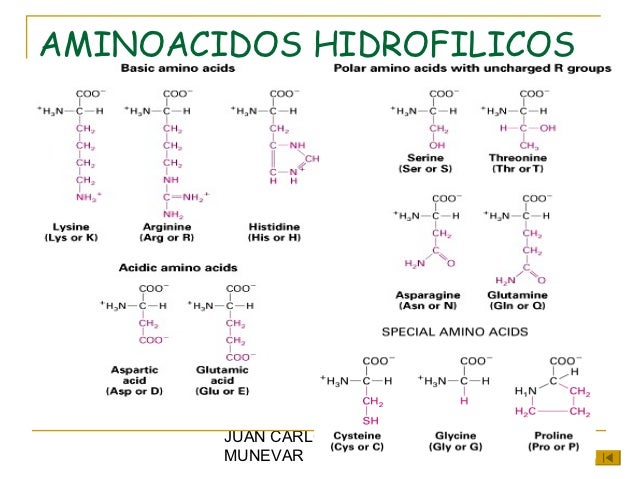
- ARN mensajero (ARNm): conocido como ARN codificante, posee el código genético que determina el esquema de los aminoácidos para formar una proteína;
- ARN transferencia (ARNt): se encarga de llevar los aminoácidos a los ribosomas con el fin de incorporarlos al proceso de síntesis proteica, asimismo, se encarga de codificar la información que posee el ARN mensajero a una secuencia de proteínas y, por último,
- ARN ribosómico (ARNr): forma parte de los ribosomas y actúa en la actividad enzimática, el mismo se encarga de crear los enlaces peptídicos entre los aminoácidos del polipéptido en el proceso de síntesis de proteínas.
También cabe mencionar el ribozima, que es un tipo de ARN con función catalizadora capaz de llevar a cabo su autoduplicación cuando hay ausencia de proteínas.
Esta característica es de gran importancia, ya que tiene que ver con la hipótesis de que el ARN fue una de las primeras formas de vida, previo al ADN, y que posibilitó que se formara la primera célula, puesto que contiene información genética almacenada y puede autoduplicarse.